
Wee1是DNA损伤修复(DDR)通路的一个重要激酶,参与细胞周期的调控,在G2/M期检查点发挥关键作用。目前一些Wee1抑制剂已在多个实体瘤,尤其在具有TP53突变的肿瘤中显示了一定的临床疗效。接下来,本文将对Wee1靶点以及Wee1抑制剂研究进展进行梳理。
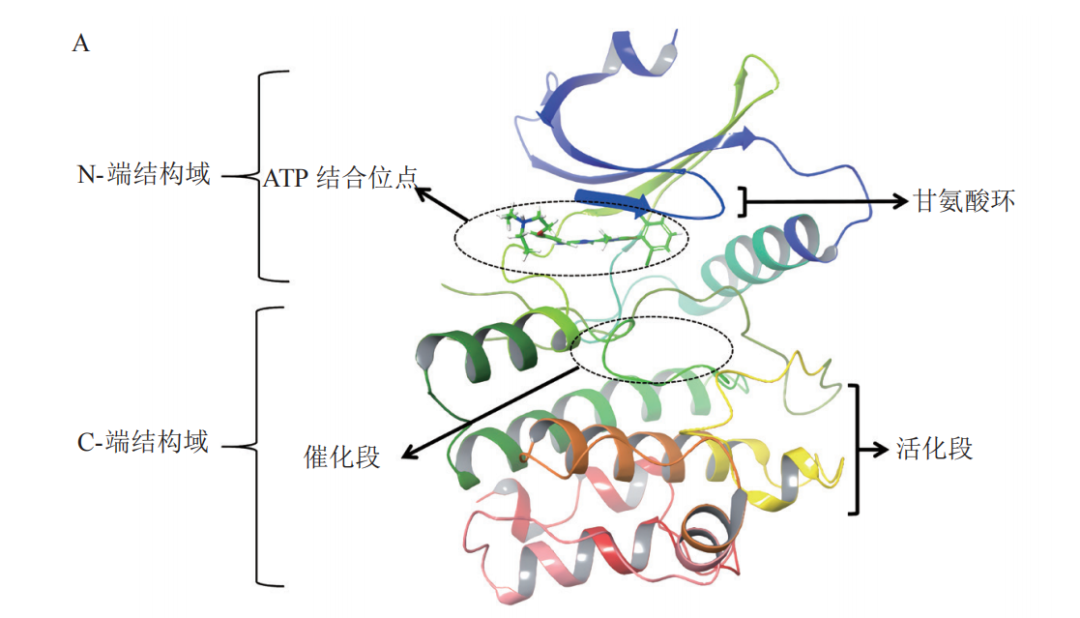
Wee1激酶最早发现于裂殖酵母中,是丝氨酸/苏氨酸蛋白激酶家族的重要成员之一,属于细胞周期调节蛋白[1]。人类的Wee1蛋白由647个氨基酸组成,主要包含3个结构域:N-端结构域、中心激酶结构域和1个短的C-端结构域。N-端结构域是Wee1激酶的激活结构域,也是抑制周期蛋白依赖性激酶 1-周期蛋白B(cyclin-dependent kinase 1-cyclin B,CDK1-CyclinB)复合物去磷酸化的潜在位点,包含1个富含甘氨酸环(残基序列 306 ~ 311)和3段富含脯氨酸、谷氨酰胺、丝氨酸、苏氨酸的序列(残基序列 24~126),这些泛素化识别位点可以严格控制Wee1的细胞内半衰期。C-端结构域主要包含催化段(残基序列 422 ~ 433)和活化段(残基序列 462~486)[
Wee1激酶在细胞周期调控中的作用
细胞周期在细胞分裂过程中被高度调控。细胞周期分为分裂间期和分裂期,DNA复制和蛋白质合成在间期完成。在细胞增殖过程中,多种原因导致DNA损伤和染色体变异。为保证基因组的完整,间期主要通过3个细胞周期检查点(G1/S 检查点、S检查点、G2/M检查点)对此进行负反馈调节,及时中断细胞周期进程[3]。Wee1主要定位于细胞核,协助并确保DNA复制过程正确。Wee1负调节作用于CDK1-Cyclin B复合物,该复合物一旦激活,细胞就会进入有丝分裂过程。在S期,Wee1激酶作为“染色质合成传感器”,有两个连续的磷酸化事件,一是在整个细胞S期磷酸化CDK1的Tyr15位点,防止细胞进入下一个细胞周期,直到DNA复制或修复完成;二是磷酸化组蛋白H2B的Tyr37位点,终止组蛋白合成,在进入有丝分裂期前维持正确的组蛋白与DNA比例。由于DNA合成与组蛋白转录的耦合对染色体形成至关重要,因此这两个过程使Wee1蛋白激酶成为维持染色体完整性的主要调节者[4]。
Wee1激酶在DNA损伤修复中的作用
真核细胞依赖复杂的细胞周期检查点和DNA修复系统确保基因组的稳定性,在细胞DNA 受到化学性或放射性损伤后,细胞周期检查点被激活,阻止细胞周期进程而使DNA进行修复。
DNA发生单链断裂,ATR信号通路激活,细胞周期检查点激酶 1(checkpoint kinase 1,Chk1)的317位和345位丝氨酸经磷酸化而激活,活化后的Chk1同时磷酸化Cdc25C(cyclin 25 homologous protein C,周期蛋白 25 同源蛋白 C)和 Wee1。Wee1激酶通过2条途径阻滞有丝分裂,包括S阻滞和G2/M 阻滞,为修复受损DNA争取时间,维持染色质的完整性。DNA修复完成后,PLK1磷酸化Wee1激酶,通过泛素连接酶降解Wee1,同时,Chk1对Cdc25C抑制作用丧失,CDK1随后被Cdc25C去磷酸化并重新激活,驱动细胞进入分裂期。
DNA发生双链断裂,ATM信号通路激活,细胞周期检查点激酶2(checkpoint kinase 2,Chk2)磷酸化Cdc25C的216位丝氨酸,促进Cdc25C 与14-3-3 蛋白结合,致使Cdc25C与细胞质分离,从而抑制其活性,进而抑制 CDK1-CyclinB 复合物磷酸化,抑制细胞进入分裂期[2]。

研究表明,Wee1蛋白激酶在多种恶性肿瘤中过表达,如胰腺癌[5]、恶性黑色素瘤[6]和恶性胶质瘤[7]等。抑制Wee1蛋白激酶表达可致G2检查点废除,允许细胞周期携带未修复的DNA进入有丝分裂期,引发有丝分裂灾难,最终导致细胞死亡。当TP53基因突变时,p53的G1期阻滞功能消失,使细胞完全依赖于G2/M检查点进行DNA修复。因此,G2/M检查点调节因子,如CHK1/2、PLK1及WEE1等有望成为TP53突变肿瘤的重要药物靶点。
相关新闻
◎版权作品,未经今日健康网书面授权,严禁转载,违者将被追究法律责任。
Copyright 2015-2018. 今日健康网 www.jinrijiankang.org All rights reserved.
违法和不良信息举报邮箱:jubao@jinrijiankang.org 执行主编:为民
未经过本站允许,请勿将本站内容传播或复制